新春佳节之际,中国人工智能与医学交叉领域迎来重磅突破。北京时间2月19日凌晨,国际顶级学术期刊《Nature》在线刊发上海交通大学医学院附属新华医院孙锟教授、余永国教授领衔团队与上海交通大学人工智能学院张娅教授、谢伟迪副教授领衔团队联合研究成果:全球首个可溯源智能体式罕见病诊断系统DeepRare。凭借首创的Agentic AI架构破解罕见病诊断世界性难题,诊断精度刷新世界纪录,其相关应用已服务全球600余家顶尖医疗科研机构,为全球罕见病患者点亮确诊希望,也标志着中国医工交叉创新成果站上世界舞台中央。
同一时间,上海医学科学家另一研究成果也在《Nature》刊发:脑内“精准修错”或改写神经疾病困境。项目由新华医院发育行为儿童保健科及教育部-上海市环境与儿童健康重点实验室教授李斐、副研究员杨侃团队,与上海交通大学医学院松江研究院仇子龙教授团队、复旦大学脑科学转化研究院研究员程田林团队和中国科学院分子细胞科学卓越创新中心李劲松院士团队合作完成,让全球神经发育疾病患者家庭看到了治疗的曙光。
成果一:AI诊断从“黑盒”变“透明诊室”
罕见病确诊难、漏诊率高是全球医疗领域的共同痛点,传统医疗AI常因推理过程不可追溯陷入“信任危机”。此次上海交大与新华医院联合团队协同多方科研力量攻关,为DeepRare打造了全球首创的“中枢-分身”可溯源AgenticAI架构,从三个维度实现对传统医疗AI的代际超越,让AI诊断拥有了“清晰的诊疗思路”。
在知识储备上,DeepRare打破医学数据孤岛,如同连接了全球所有顶尖医学图书馆和临床案例库,实时整合海量医学文献知识库与真实临床病例数据,不再是简单的信息检索,而是对医学知识的深度理解与内化,为每一次诊断调动全球顶尖医学储备。在诊断思维上,它跳出传统AI的“模式匹配快思考”,拥有了人类医生的“慢思考”能力,能主动提问补充患者信息,通过“假设-验证-自我反思”的迭代循环推敲诊断线索,修正逻辑漏洞,就如同资深医生反复研判病情的专业过程。在推理过程上,它实现全流程白盒推理,每一个诊断结论都附带完整证据链条,让医生既能知道诊断结果,更清楚诊断依据,彻底破解AI医疗的“信任难题”。
论文实测数据显示,在仅提供患者临床表型信息、无基因数据的情况下,DeepRare展现出超强的“表型解码”能力,表型诊断首位准确率达57.18%,较此前国际最佳模型提升23.79个百分点,这一里程碑式突破,为基层医院打造了一把罕见病快速筛查的“金钥匙”,让基层无需依赖复杂基因检测,也能开展高效的罕见病初筛。而当引入基因测序数据后,DeepRare的诊断效能进一步升级,在复杂病例中的综合首位诊断准确率突破70.6%,显著优于国际通用的Exomiser工具(53.2%)。更值得一提的是,其生成的带完整证据链的推理报告,获得了新华医院专家团队95.4%的高度认可,真正做到了诊断“有理有据、精准可靠”。
基于该成果的DeepRare罕见病在线诊断平台于2025年7月26日正式上线,凭借精准的诊断能力和便捷的使用体验,迅速获得全球医疗科研领域的认可。平台上线短短半年,已吸引超1000名专业用户注册,覆盖全球600多家医疗及科研机构,从国内的三甲医院到欧美的顶尖实验室,DeepRare正成为全球医生诊疗罕见病的“智能听诊器”。
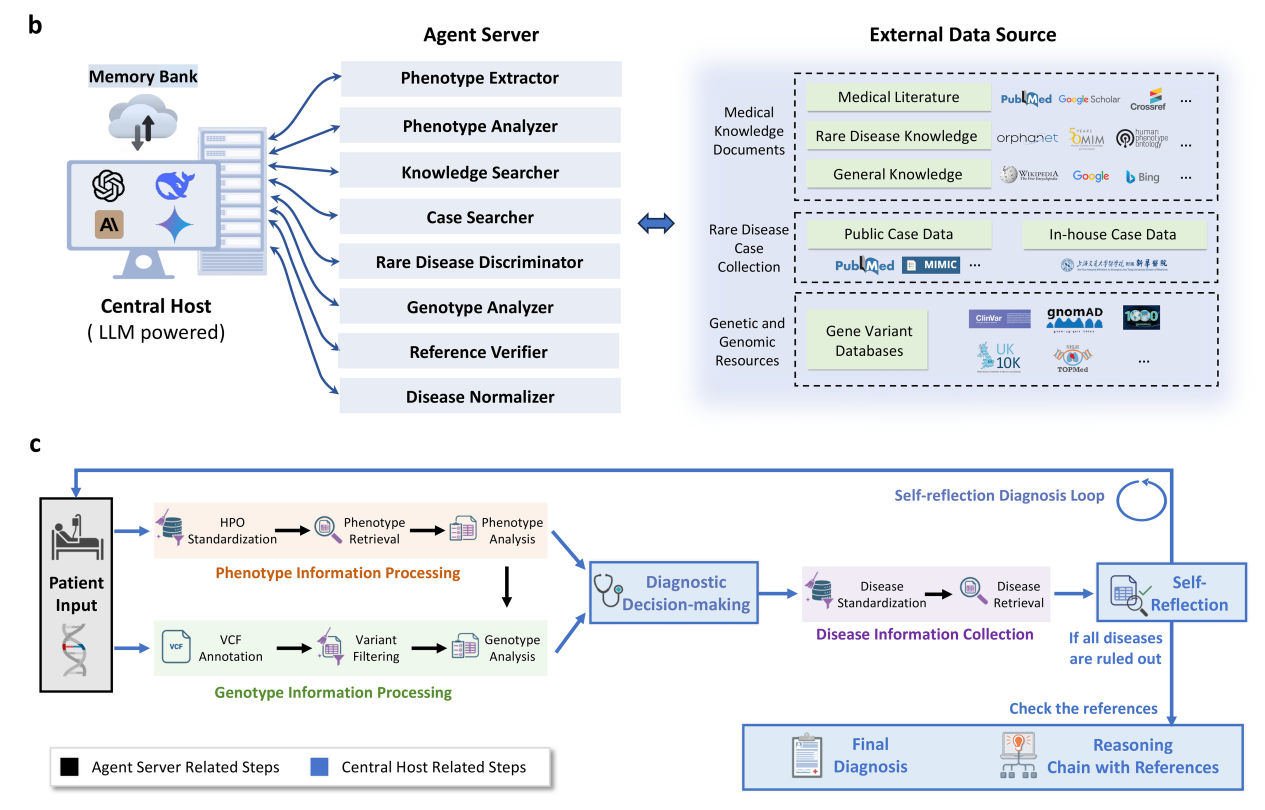
《Nature》在线发布可溯源智能体式罕见病诊断系统DeepRare。受访者供图
为将这一“中国方案”推广至全世界,让更多罕见病患者受益,新华医院与上海交大联合团队正积极筹备发起“全球AI罕见病诊疗联盟”,并同步启动“万人临床验证计划”。团队计划在未来半年内,依托全球联盟网络,完成20000例疑难罕见病的真实世界验证。
成果二:量身定制“基因工匠”,精准修正碱基错配
以自闭症为代表的神经发育性疾病长期以来“无药可用”,让患者家庭背负着沉重的身心与经济压力。李斐等研究人员聚焦Snijders Blok–Campeau综合征(SNIBCPS),一种典型的神经发育性疾病,患者出现自闭症特征、全面发育迟缓、语言障碍、智力障碍及肌张力低下等一系列问题。研究团队构建了人源化的突变小鼠模型。这些小鼠完美复刻了患者的核心症状,出现了社交回避、重复刻板动作、认知迟钝、发声异常以及运动不协调等行为异常,为后续治疗研究搭建了精准的“疾病模拟平台”。
研究团队创新性地设计了一款新型腺嘌呤碱基编辑器——TadA- embedded adenine base editor(TeABE),精准修复“出错”的基因位点。
与传统基因编辑技术可能造成DNA双链断裂的“粗犷操作”不同,这款“工匠”能精准识别并将突变的A·T碱基对修复为正常的G·C碱基对,整个过程如同在书页上修正单个错字,不会破坏DNA的整体结构,大幅降低了基因编辑过程中可能出现的基因组紊乱风险。
在完成实验室筛选后,研究团队通过尾静脉注射的方式,将这款定制“基因编辑器”送入突变小鼠体内。令人振奋的是,编辑器成功抵达小鼠多个脑区,实现了精准的靶向修复,且几乎没有对周围正常基因造成影响(较低的旁观者效应)。
更关键的是,随着CHD3蛋白水平显著恢复,小鼠的行为异常也得到了直接的改善。在三箱社交实验中,原本回避同伴的小鼠开始主动与同类互动;在新物体识别实验中,它们能清晰分辨新物体与熟悉物体,认知缺陷得到缓解;在巴恩斯迷宫学习实验中,其学习和记忆能力也恢复正常。同时,小鼠的运动能力也同步提升,肌张力增强,原本不协调的步态变得稳健。
为了确保这款“基因编辑器”的安全性,研究团队通过GUIDE-seq技术在全基因组范围内“排查”可能的脱靶位点。结果显示,在人类细胞中潜在的脱靶位点编辑率均低于1%,在小鼠脑中这一数值更低,几乎可以忽略不计。此外,研究团队还对编辑过程中可能产生的次要突变进行了功能验证,确认这些微小突变不会影响CHD3蛋白的正常功能,进一步为治疗的安全性筑牢了防线。
要让基因治疗真正走向人类临床,还需证明其在更接近人类的动物模型中同样安全有效。为此,研究团队在非人灵长类(猕猴)模型中开展了鞘内注射AAV9-TeABE实验。结果显示,编辑器在猕猴脑内高效表达并完成拼接,成功检测到明确的碱基编辑活性。这一成果不仅证明了该技术具备跨物种应用的可行性,更为后续临床试验积累了充足的前期数据。
《Nature》发布自闭症“基因编辑器”。受访者供图
研究人员坦言,从动物模型到人类临床治疗,还有很长的路要走。目前,研究团队已在规划下一步实验,包括优化编辑器结构、探索更安全的递送方式、建立人源类器官疾病模型以及构建大型动物长期安全性评价体系等。希望不久的将来,基于碱基编辑的基因治疗策略将为更多神经发育疾病患者带来希望。
头图为DeepRare系统推理架构图。新华医院供图

